La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) dispuso la prohibición de venta, uso y distribución en todo el territorio argentino de un bótox sin autorización sanitaria y de un fármaco promocionado para tratar la diabetes y favorecer el descenso de peso, luego de detectar que ninguno de los dos productos contaba con inscripción oficial en el registro correspondiente. La decisión quedó plasmada en dos disposiciones publicadas este martes en el Boletín Oficial y firmadas por el titular del organismo, Luis Eduardo Fontana.
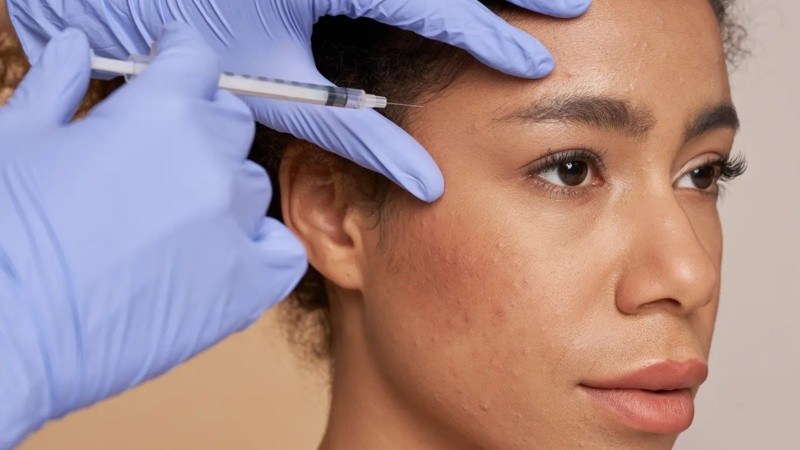
La primera resolución, identificada con el número 2325/2026, alcanza a la denominada “Toxina botulínica ISRADERM”, utilizada habitualmente en procedimientos médicos y estéticos similares al bótox. Desde el organismo nacional señalaron que, tras las verificaciones realizadas, se constató que el producto no figura inscripto en el Registro de Especialidades Medicinales.
En el texto oficial, la Anmat recordó que en el país sí existen medicamentos elaborados a base de toxina botulínica debidamente habilitados, aunque subrayó que su expendio está permitido únicamente bajo receta archivada y a través de farmacias autorizadas. En consecuencia, advirtió que cualquier modalidad de comercialización por fuera de esos canales implica un serio riesgo para la salud pública.
A partir de ello, el organismo sostuvo que el producto cuestionado no podía ser ofrecido de la manera en que fue detectado y remarcó que, al tratarse de un medicamento sin registro, su circulación y utilización están terminantemente prohibidas.
Además, alertó que se desconoce cuál es su origen legítimo, por lo que no es posible garantizar estándares mínimos de calidad, seguridad ni eficacia, situación que lo convierte en un potencial peligro para quienes pudieran consumirlo o aplicárselo.
Por ese motivo, resolvió vetar en todo el país todas las partidas y presentaciones de la “Toxina botulínica ISRADERM” hasta tanto obtenga las autorizaciones sanitarias exigidas por la normativa vigente.
La segunda disposición, la 2369/2026, recae sobre el producto “Lipoless 2,5 mg / Tirzepatida 2,5 mg/0,6 ml”, difundido como un tratamiento indicado para pacientes con diabetes tipo 2 y también para el control del peso corporal.
Según precisó la Anmat, durante la investigación se corroboró que este medicamento tampoco se encuentra incorporado al Registro de Especialidades Medicinales, condición indispensable para poder comercializarse legalmente en la Argentina.
En la disposición se recordó asimismo que en el mercado nacional ya existe una especialidad medicinal autorizada cuyo principio activo es la tirzepatida, pero que, al igual que otros fármacos de este tipo, solo puede venderse bajo receta. En ese marco, el organismo advirtió que su promoción y oferta mediante redes sociales o plataformas digitales representa un elevado riesgo sanitario.
En línea con el caso anterior, el ente de control concluyó que el producto detectado no podía comercializarse en esas condiciones y reiteró que, al no contar con habilitación oficial, su uso y distribución quedan prohibidos.
Finalmente, ordenó retirar del mercado y prohibir en todo el territorio nacional todos los lotes y presentaciones de “Lipoless 2,5 mg / Tirzepatida 2,5 mg/0,6 ml” hasta que reúna las autorizaciones sanitarias correspondientes.